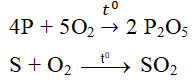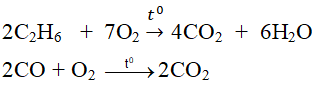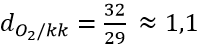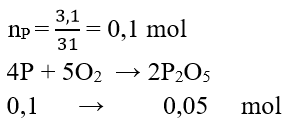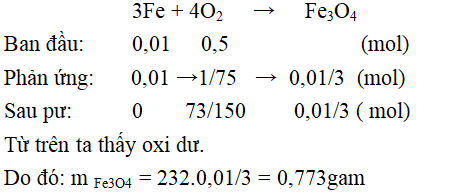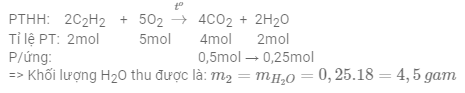Mời các em theo dõi nội dung bài học về Nêu tính chất hóa học của oxi, viết phương trình minh họa dễ hiểu do thầy cô trường THCS Bình Chánh biên soạn. Hy vọng sẽ là tài liệu hữu ích giúp các em học tốt và hoàn thành tốt bài tập của mình.
Mục lục
Nêu tính chất hóa học của oxi, viết phương trình minh họa
Câu hỏi: Nêu tính chất hóa học của oxi, viết phương trình minh họa.
Trả lời: Khí oxi là một đơn chất phi kim rất hoạt động, đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim, nhiều kim loại và hợp chất. Trong các hợp chất hóa học, nguyên tố oxi có hóa trị II.
Cụ thể:
– Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt.
Ví dụ:
– Tác dụng với hiđro, phản ứng có thể gây nổ mạnh nếu tỉ lệ thể tích O2 : H2 = 1:2
Phương trình hóa học:
– Tác dụng với một số phi kim khác:
Ví dụ:
+ Tác dụng với một số hợp chất:
Ví dụ:

Bài tập về tính chất hóa học của oxi
Câu 1: Khí oxi nặng hơn không khí bao nhiêu lần
A. 1,1 lần
B. 0,55 lần
C. 0,90625 lần
D. 1,8125 lần
Lời giải:
Đáp án: A
Câu 2: Đốt cháy 3,1 g photpho trong bình chứa oxi tạo ra điphotpho pentaoxit. Tính khối lượng oxit thu được
A. 1,3945 g
B. 14,2 g
C. 1,42 g
D. 7,1 g
Lời giải:
Đáp án: D
mP2O5= 0,05.142 = 7,1 g
Câu 3: Cháy mạnh, sáng chói, không có khói là hiện tượng của phản ứng
A. C+O2 → CO2
B. 3Fe+2O2 → Fe3O4
C. 2Cu+O2 → 2CuO
D. 2Zn+O2 → 2ZnO
Lời giải:
Đáp án: B
Câu 4: Cháy trong oxi với lửa nhỏ có màu xanh nhạt, cháy trong không khí mãnh liệt hơn là hiện tượng của phản ứng
A. 2S + 3O2 → 2SO3
B. S + O2 → SO2
C. P + O2 → P2O5
D. P + O2 →P2O5
Lời giải:
Đáp án: A
Câu 5: Cháy mạnh trong oxi với ngọn lửa sáng chói, tạo ra khói trắng dày đặc bám vào thành lọ dưới dạng bột hòa tan được nước là phản ứng
A. 4P + 5O2 → 2P2O5
B. P + O2 → P2O3
C. S + O2 →SO2
D. 2Zn + O2 →2 ZnO
Lời giải:
Đáp án: A
Câu 6: Cho 0,56 g Fe tác dụng với 16 g oxi tạo ra oxit sắt từ. Tính khối lượng oxit sắt từ và cho biết chất còn dư sau phản ứng
A. Oxi dư và m = 0,67 g
B. Fe dư và m = 0,774 g
C. Oxi dư và m = 0,773 g
D. Fe dư và m = 0,67 g
Lời giải:
Đáp án: C
nFe = 0,56/56 = 0,01 mol, nO2 = 16/32 = 0,5 mol
Câu 7: Tính chất nào sau đây oxi không có
A. Oxi là chất khí
B. Trong các hợp chất, oxi có hóa trị 2
C. Tan nhiều trong nước
D. Nặng hơn không khí
Lời giải:
Đáp án: C
Câu 8: Chọn đáp án đúng
A. Oxi không có khả năng kết hợp với chất hemoglobin trong máu
B. Khí oxi là một đơn chất kim loại rất hoạt động
C. Oxi nặng hơn không khí
D. Oxi có 3 hóa trị
Lời giải:
Đáp án: C
Câu 9: Chọn đáp án đúng
A. CH4 + O2 → 2CO2 + H2O
B. 2C2H2 +5O2→ 4CO2 + 2H2O
C. Ba + O2 → BaO
D. 2KClO3 → 2KCl + O2
Lời giải:
Đáp án: B
Câu 10: Tính thể tích khí oxi phản ứng khi đốt cháy 3,6 g C
A. 0,672 l
B. 67,2 l
C. 6,72 l
D. 0,0672 l
Lời giải:
Đáp án: C
C + O2 → CO2
nC = 3,6/12 = 0,3 mol
nhìn vào phương trình thấy số mol của C bằng số mol oxi phản ứng
⇒ VO2 = 0,3.22,4 = 6,72 l
Câu 11: Đốt cháy m1 gam kẽm bằng khí oxi vừa đủ, thu được 12,15 gam ZnO. Hòa tan toàn bộ lượng ZnO ở trên vào dung dịch chứa m2 gam HCl vừa đủ thu được sản phẩm là ZnCl2 và nước. Tính m1 + m2
A. 20,7 gam.
B. 10,95 gam.
C. 9,75 gam.
D. 10,35 gam
Lời giải:
Số mol ZnO thu được là: nZnO = =0,15 mol
PTHH: 2Zn + O2 2ZnO
Tỉ lệ PT: 2mol 1mol 2mol
Phản ứng: 0,15mol ← 0,15mol
=> Khối lượng Zn phản ứng là: m1 = mZn = 0,15.65 = 9,75 gam
Lấy 0,15 mol ZnO cho vào dung dịch HCl
PTHH: ZnO + 2HCl → ZnCl2 + H2O
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,15mol → 0,3mol
=> Khối lượng HCl phản ứng là: mHCl = m2 = 0,3.36,5 = 10,95 gam
=> m1 + m2 = 9,75 + 10,95 = 20,7 gam
Đáp án cần chọn là: A
Câu 12: Đốt cháy hoàn toàn 32 gam khí metan (CH4) cần V lít khí oxi (đktc), thu được khí CO2 và H2O. Giá trị của V là
A. 22,4 lít.
B. 89,6 lít.
C. 44,8 lít.
D. 67,2 lít.
Lời giải:
Số mol khí CH4 là: nCH4= =2 mol
PTHH: CH4 + 2O2 CO2 + 2H2O
Tỉ lệ PT: 1mol 2mol
Phản ứng: 2mol → 4mol
=> thể tích khí oxi cần dùng là: VO2 = 22,4.n = 22,4.4 = 89,6 lít
Đáp án cần chọn là: B
Câu 13: Đốt cháy hoàn toàn m1 gam khí etilen (C2H4) cần 7,392 lít khí oxi (đktc), thu được m2 gam khí CO2 và m3 gam H2O. Tính m1 + m2 + m3
A. 19,36 gam.
B. 10,59 gam.
C. 10,12 gam.
D. 16,72 gam.
Lời giải:
Số mol khí O2 là: nO2 = =0,33mol
Ta có PTHH: C2H4 + 3O2 2CO2 + 2H2O
Theo phương trình cứ 3 mol O2 thì đốt cháy hết 1 mol C2H4
Theo đầu bài………………0,33 mol O2…… = 0,11mol C2H4
Áp dụng định luật bảo toàn khối lượng ta có: m C2H4 + mO2 = mCO2 + mH2O
=> mCO2 + mH2O = 0,11.28 + 0,33.32=13,64
=> m1 + m2 + m3 = m C2H4 + mCO2 + mH2O = 13,64 + 3,08= 16,72 gam
Đáp án cần chọn là: D
Câu 14: Đốt cháy 7,8 gam khí axetilen (C2H2) trong khí oxi, thu được 11,2 lít khí CO2 (đktc) và m2 gam H2O. Giá trị m2 là
Lời giải:
Số mol khí C2H2 là: nC2H2 = =0,3mol
Số mol khí CO2 là: nCO2 = =0,5mol
Vì đầu bài cho 2 số liệu số mol của chất phản ứng C2H2 và chất sản phẩm CO2 => tính toán theo chất sản phẩm
Đáp án cần chọn là: C
Câu 15: Khí được con người sử dụng để hô hấp là:
A. H2.
B. O2.
C. N2.
D. CO2.
Lời giải:
Con người hít khí O2 vào cơ thể để hô hấp
Đáp án cần chọn là: B
***
Trên đây là nội dung bài học Nêu tính chất hóa học của oxi, viết phương trình minh họa dễ hiểu do thầy cô trường THCS Bình Chánh biên soạn và tổng hợp. Hy vọng sẽ giúp các em hiểu rõ nội dung bài học và từ đó hoàn thành tốt bài tập của mình. Đồng thời luôn đạt điểm cao trong các bài thi bài kiểm tra sắp tới. Chúc các em học tập thật tốt.
Đăng bởi THCS Bình Chánh trong chuyên mục Học tập