Khoa học tự nhiên 7 Bài 3 Cánh diều: Sơ lược về bảng tuần hoàn các nguyên tố hóa học | Giải KHTN 7
Mời các em theo dõi nội dung bài học do thầy cô trường Trung học Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn.
Giải bài tập Khoa học tự nhiên 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Bạn đang xem: Khoa học tự nhiên 7 Bài 3 Cánh diều: Sơ lược về bảng tuần hoàn các nguyên tố hóa học | Giải KHTN 7
Bài giảng Khoa học tự nhiên 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Mở đầu trang 19 Bài 3 KHTN lớp 7: Ai nhanh hơn?
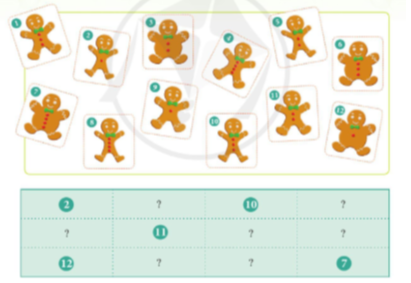
Hãy sắp xếp những tấm thẻ vào các ô trong bảng dưới đây theo quy luật nhất định.
Hãy cho biết các tấm thẻ được sắp xếp theo quy luật nào theo hàng và theo cột.
Tương tự như vậy, có thể sắp xếp các nguyên tố hóa học theo quy luật vào một bảng được không?
Trả lời:
Các tấm thẻ được sắp xếp như sau:
|
(2) |
(5) |
(10) |
(8) |
|
(9) |
(11) |
(1) |
(4) |
|
(12) |
(3) |
(6) |
(7) |
+ Theo hàng ngang từ trái sang phải các tấm thẻ được sắp xếp theo quy luật: Các chú gấu trong tấm thẻ có kích thước bằng nhau, số khuy áo của các chú gấu tăng dần.
+ Theo cột từ trên xuống dưới các tấm thẻ được sắp xếp theo quy luật: Các chú gấu trong tấm thẻ có cùng số khuy áo, kích thước các chú gấu tăng dần.
– Tương tự như vậy, nếu coi các khuy áo là những electron, kích thước chú gấu tăng dần như số lớp electron tăng dần ta có thể sắp xếp các nguyên tố hóa học theo quy luật vào một bảng.
I. Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
Câu hỏi 1 trang 20 KHTN lớp 7: Cho biết điện tích hạt nhân của mỗi nguyên tử C, Si, O, P, N, S lần lượt là 6, 14, 8, 15, 7, 16. Hãy sắp xếp các nguyên tố trên theo chiều điện tích hạt nhân tăng dần từ trái sang phải và từ trên xuống dưới.
|
C |
? |
O |
|
Si |
? |
? |
Trả lời:
Sắp xếp các nguyên tố theo chiều điện tích hạt nhân tăng dần từ trái sang phải và từ trên xuống dưới như sau:
|
C (6) |
N (7) |
O (8) |
|
Si (14) |
P (15) |
S (16) |
Tìm hiểu thêm trang 20 KHTN lớp 7: Việc tìm ra bảng tuần hoàn là một trong những phát hiện xuất sắc nhất trong ngành hóa học. Em hãy tìm hiểu lịch sử phát minh ra bảng tuần hoàn các nguyên tố hóa học.
Trả lời:
Ngay từ khi chưa biết rõ về cấu tạo nguyên tử, các nhà khoa học đã tìm ra cách phân loại, sắp xếp các nguyên tố hóa học để tìm ra quy luật về tính chất của chúng. Trong lịch sử nghiên cứu, một số quy luật sắp xếp đã được tìm ra nhưng đều không thành công.
+ Cách phân loại đầu tiên được A. Lavoiser thực hiện năm 1789, xếp 33 nguyên tố hóa học thành nhóm các chất khí, kim loại, phi kim và “đất”.
+ Năm 1829, J. W. Dobereiner phân loại các nguyên tố thành các nhóm có tính chất hóa học giống nhau.
Ví dụ: lithium, sodium và potassium là nhóm các kim loại mềm, dễ phản ứng.
+ Năm 1866, J. Newlands đã xếp các nguyên tố hóa học theo chiều tăng khối lượng nguyên tử thành các octave (quãng tám), trong đó nguyên tố thứ tám lặp lại tính chất của nguyên tố đầu tiên.
+ Năm 1869, hai nhà hóa học, D. I. Mendeleev và J. L. Meyer đều sắp xếp các nguyên tố theo chiều tăng khối lượng nguyên tử vào các hàng và cột, bắt đầu mỗi hàng (bảng của Mendeleev) hoặc cột mới (bảng của Mayer) khi các tính chất của nguyên tố bắt đầu lặp lại. Trong bảng tuần hoàn của mình, Mendeleev đã thay đổi vị trí một số nguyên tố để tính chất của nguyên tố phù hợp với quy luật, đồng thời để trống một số chỗ cho các nguyên tố chưa biết.
– Sau này, các nguyên tố hóa học ở vị trí còn trống đó được tìm ra và tính chất của chúng đều phù hợp với dự đoán của Mendeleev.
II. Cấu tạo bảng tuần hoàn
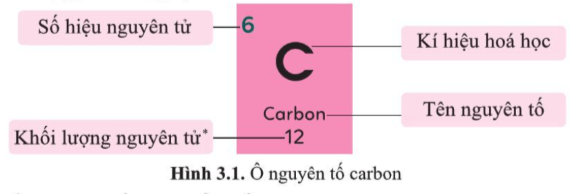
Câu hỏi 2 trang 20 KHTN lớp 7: Hình 3.1 cho biết các thông tin gì về nguyên tố carbon?
Trả lời:
Hình 3.1 cho biết:
+ Tên nguyên tố là carbon.
+ Số hiệu nguyên tử của nguyên tố carbon là Z = 6.
+ Kí hiệu hóa học là C.
+ Khối lượng nguyên tử của nguyên tố carbon bằng 12 (amu).
Luyện tập 1 trang 20 KHTN lớp 7: Hãy tìm nguyên tố hóa học có số thứ tự lần lượt là 16 và 20 trong bảng tuần hoàn. Đọc tên hai nguyên tố. Hãy cho biết số hiệu nguyên tử, kí hiệu hóa học và khối lượng nguyên tử của hai nguyên tố đó.
Trả lời:
Dựa vào bảng tuần hoàn các nguyên tố hóa học trang 25 – SGK Khoa học tự nhiên 7 – Cánh diều ta có:
– Nguyên tố hóa học có số thứ tự 16 là sulfur (lưu huỳnh):
+ Số hiệu nguyên tử: Z = 16
+ Kí hiệu hóa học: S
+ Khối lượng nguyên tử: 32 (amu).
– Nguyên tố hóa học có số thứ tự 20 là calcium:
+ Số hiệu nguyên tử: Z = 20
+ Kí hiệu hóa học: Ca
+ Khối lượng nguyên tử: 40 (amu)
Câu hỏi 3 trang 21 KHTN lớp 7: Quan sát bảng tuần hoàn, cho biết số hiệu nguyên tử lần lượt của nguyên tử carbon (C) và aluminium (Al). Hai nguyên tố đó nằm ở chu kì nào trong bảng tuần hoàn? Từ đó cho biết số lớp electron của C và Al
Trả lời:
Để trả lời câu hỏi này các em cần nhớ:
+ Số hiệu nguyên tử của nguyên tố Z = số proton = số electron.
+ Số thứ thự chu kì = số lớp electron.
|
Nguyên tử |
Số hiệu nguyên tử |
Số lớp electron |
Chu kỳ |
|
Carbon (C) |
6 |
2 |
2 |
|
Aluminium (Al) |
13 |
3 |
3 |
Luyện tập 2 trang 21 KHTN lớp 7: Nguyên tố X có số thứ tự 15 trong bảng tuần hoàn. Hãy cho biết nguyên tố đó ở chu kì nào và có mấy lớp electron.
Trả lời:
Cách 1:
– Nguyên tử X có số thứ tự 15 = số hiệu nguyên tử Z = số proton = số electron.
⇒ Các electron được sắp xếp vào 3 lớp:
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 8 electron.
+ Lớp thứ ba có 5 electron
⇒ Nguyên tố X nằm ở chu kì 3 trong bảng tuần hoàn.
Cách 2:
Quan sát bảng tuần hoàn, xác định được nguyên tố có số thứ tự 15 ở chu kì 3 của bảng tuần hoàn.
⇒ X có 3 lớp electron (do số thứ tự chu kì = số lớp electron).
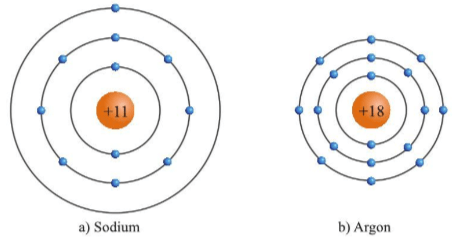
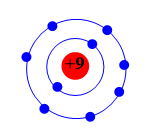
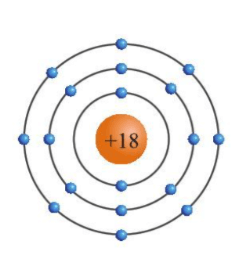
Luyện tập 3 trang 21 KHTN lớp 7:Dựa vào hình 3.4, hãy cho biết một số thông tin về nguyên tố sodium và argon (số hiệu nguyên tử, điện tích hạt nhân, số lớp electron, chu kì, số electron ở lớp ngoài cùng).
Hình 3.4. Mô hình cầu tạo nguyên tử sodium và argon
Trả lời:
|
Nguyên tố |
Số hiệu nguyên tử (Z) |
Điện tích hạt nhân |
Số lớp electron |
Chu kì |
Số electron ở lớp ngoài cùng |
|
Sodium (Na) |
11 |
+11 |
3 |
3 |
1 |
|
Argon (Ar) |
18 |
+18 |
3 |
3 |
8 |
Luyện tập 4 trang 22 KHTN lớp 7: Nguyên tố X tạo nên chất khí duy trì sự hô hấp của con người, động vật và thực vật và có nhiều trong không khí. Hãy cho biết tên của nguyên tố X. Nguyên tố X nằm ở ô nào và chu kì nào trong bảng tuần hoàn?
Trả lời:
Nguyên tố oxygen (O) tạo nên khí oxygen (O2) duy trì sự hô hấp của con người, động vật, thực vật và có nhiều trong không khí (chiếm khoảng 21% thể tích không khí).
– Tên nguyên tố: Oxygen
– Kí hiệu hóa học: O
– Dựa vào bảng tuần hoàn hóa học xác định được nguyên tố O nằm ở ô số 8 và chu kì 2 trong bảng tuần hoàn.
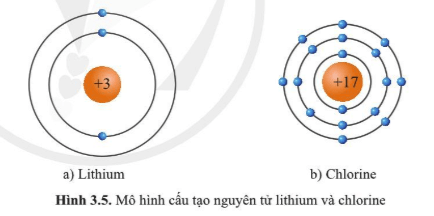
Câu hỏi 4 trang 22 KHTN lớp 7: Quan sát hình 3.5 và bảng tuần hoàn, hãy cho biết số electron lớp ngoài cùng của nguyên tử Li (lithium) và Cl (chlorine). Hai nguyên tố đó nằm ở nhóm nào trong bảng tuần hoàn?
Trả lời:
Quan sát hình 3.5 và bảng tuần hoàn xác định được:
– Nguyên tử Li (lithium) có 1 electron lớp ngoài cùng. Nguyên tử Li (lithium) nằm ở nhóm IA trong bảng tuần hoàn.
– Nguyên tử Cl (chlorine) có 7 electron lớp ngoài cùng. Nguyên tử Cl (chlorine) nằm ở nhóm VIIA trong bảng tuần hoàn.
Lưu ý: Số thứ tự nhóm A = số electron lớp ngoài cùng.
Luyện tập 5 trang 23 KHTN lớp 7: Cho các nguyên tố có số thứ tự lần lượt là 9, 18 và 19. Số electron lớp ngoài cùng của mỗi nguyên tố trên là bao nhiêu? Cho biết mỗi nguyên tố nằm ở nhóm nào và đó là kim loại, phi kim hay khí hiếm.
Trả lời:
Xét nguyên tố có số thứ tự 9:
– Số thứ tự = 9 = số hiệu nguyên tử Z = số proton = số electron.
– Các electron được sắp xếp vào 2 lớp ⇒ Nguyên tố nằm ở chu kì 2 trong bảng tuần hoàn.
– Lớp ngoài cùng có 7 electron ⇒ Nguyên tố thuộc nhóm VIIA, là phi kim.
Xét nguyên tố có số thứ tự 18:
– Số thứ tự = 18 = số hiệu nguyên tử Z = số proton = số electron.
– Các electron được sắp xếp vào 3 lớp ⇒ Nguyên tố nằm ở chu kì 3 trong bảng tuần hoàn.
– Có 8 electron lớp ngoài cùng ⇒ Nguyên tố thuộc nhóm VIIIA, là khí hiếm.
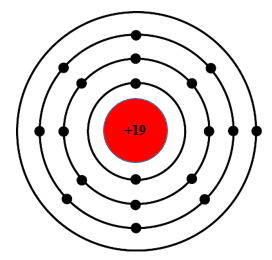
Xét nguyên tố có số thứ tự 19:
– Số thứ tự = 19 = số hiệu nguyên tử Z = số proton = số electron.
Các electron được xếp vào 4 lớp, lớp ngoài cùng có 1 electron ⇒ Nguyên tố thuộc chu kì 4, nhóm IA trong bảng tuần hoàn, là kim loại.
Chú ý: Học sinh có thể quan sát trực tiếp bảng tuần hoàn để xác định.
Tìm hiểu thêm trang 23 KHTN lớp 7: Ngoài 8 nhóm A, bảng tuần hoàn còn có nhóm B. Em hãy hiểu về các nhóm B
Trả lời:
– Nhóm B (còn gọi là nhóm các nguyên tố kim loại chuyển tiếp) gồm 8 nhóm được đánh số từ IIIB đến VIIIB, rồi IB và IIB theo chiều từ trái sang phải trong bảng tuần hoàn.
– Nhóm B gồm 10 cột, riêng nhóm VIIIB gồm 3 cột.
– Nhóm B chỉ gồm các nguyên tố của các chu kỳ lớn (từ chu kì 4 trở đi).
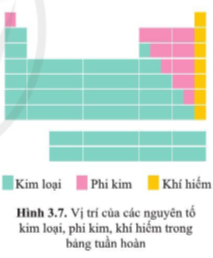
III. Vị trí của các nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn:
Câu hỏi 5 trang 23 KHTN lớp 7: Quan sát bảng tuần hoàn các nguyên tố hóa học, hãy cho biết vị trí của các nguyên tố kim loại, phi kim và khí hiếm.
Trả lời:
– Các nguyên tố kim loại nằm ở phía bên trái và góc dưới bên phải của bảng tuần hoàn. (ô nguyên tố màu xanh trong bảng tuần hoàn).
– Các nguyên tố phi kim nằm ở phía trên, bên phải của bảng tuần hoàn. (ô nguyên tố màu hồng trong bảng tuần hoàn).
– Các nguyên tố khí hiếm là tất cả các nguyên tố nằm trong nhóm VIIIA. (ô nguyên tố màu vàng cam trong bảng tuần hoàn).
IV. Ý nghĩa của bảng tuần hoàn
Câu hỏi 6 trang 24 KHTN lớp 7: Nguyên tố X nằm ở chu kì 2, nhóm VA trong bảng tuần hoàn. Hãy cho biết một số thông tin của nguyên tố X (tên nguyên tố, kí hiệu hóa học, khối lượng nguyên tử), vị trí của ô nguyên tố trong bảng tuần hoàn. Nguyên tố đó là kim loại, phi kim hay khí hiếm?
Trả lời:
Nguyên tố X nằm ở chu kì 2, nhóm VA trong bảng tuần hoàn.
Ta biết được:
– Tên nguyên tố X là: Nitrogen.
– Kí hiệu hóa học: N
– Khối lượng nguyên tử: 14 (amu).
– X ở ô thứ 7 trong bảng tuần hoàn, là nguyên tố phi kim.
Vận dụng trang 24 KHTN lớp 7: Hãy tự thiết kế bảng tuần hoàn với 3 chu kì và 8 nhóm bằng các tấm thẻ (bìa) cho 18 nguyên tố có số thứ tự từ 1 đến 18 với các thông tin mà em biết. Tô màu để phân biệt các nguyên tố kim loại, phi kim, khí hiếm.
Trả lời:
Học sinh tự nghiên cứu, thiết kế, có thể tham khảo một số ý tưởng sau:
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Bài tập Chủ đề 1, 2
Bài 4: Phân tử, đơn chất, hợp chất
Bài 5: Giới thiệu về liên kết hóa học
Bài 6: Hóa trị, công thức hóa học
Bài tập Chủ đề 3
Xem thêm tài liệu Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Lý thuyết Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Đăng bởi: THCS Bình Chánh
Chuyên mục: Khoa học tự nhiên 7 Cánh Diều
- Khoa học tự nhiên 7 Bài mở đầu Cánh diều: Phương pháp và kĩ năng trong học tập môn khoa học tự nhiên | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 1 Cánh diều: Nguyên tử | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 2 Cánh diều: Nguyên tố hóa học | Giải KHTN 7
- Khoa học tự nhiên 7 Cánh diều Bài tập Chủ đề 1, 2 trang 26, 27 | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 4 Cánh diều: Phân tử, đơn chất, hợp chất | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 5 Cánh diều: Giới thiệu về liên kết hóa học | Giải KHTN 7