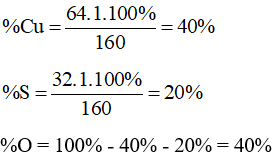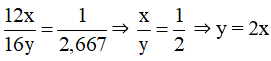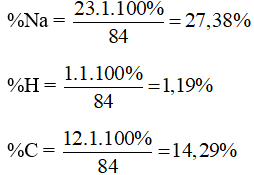Khoa học tự nhiên 7 Bài 7 Kết nối tri thức: Hóa trị và công thức hóa học | Giải KHTN 7
Mời các em theo dõi nội dung bài học do thầy cô trường Trung học Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn.
Giải bài tập Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học
Bạn đang xem: Khoa học tự nhiên 7 Bài 7 Kết nối tri thức: Hóa trị và công thức hóa học | Giải KHTN 7
Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học
A/ Câu hỏi đầu bài
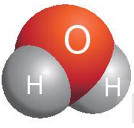
Mở đầu trang 40 Bài 7 Khoa học tự nhiên 7: Trong phân tử nước, một nguyên tử O liên kết với hai nguyên tử H, người ta nói rằng O có hóa trị II. Vậy hóa trị có mối liên hệ với công thức hóa học của hợp chất như thế nào?
Lời giải:
– Trong công thức hóa học của hợp chất hai nguyên tố, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
– Người ta quy ước nguyên tố H luôn có hóa trị I. Nguyên tử của nguyên tố khác liên kết được với bao nhiêu nguyên tử H thì nguyên tố đó có hóa trị bằng bất nhiêu.
– Oxygen cũng được quy ước có hóa trị II. Từ đó ta xác định được hóa trị cho các nguyên tố khác trong các hợp chất có chứa H hoặc O.
B/ Câu hỏi giữa bài
I. Công thức hóa học
Giải KHTN 7 trang 41
Câu hỏi trang 41 Khoa học tự nhiên 7: Copper sulfate (CuSO4) được dùng làm chất chống xoăn lá cây cho cây cà chua. Em hãy cho biết số nguyên tử của từng nguyên tố có trong một phân tử copper sulfate và xác định phần trăm khối lượng của các nguyên tố trong hợp chất này.
Lời giải:
Trong một phân tử copper sulfate (CuSO4) có một nguyên tử Cu, một nguyên tử S và bốn nguyên tử O.
Khối lượng phân tử CuSO4 bằng: 64.1 + 32.1 + 16.4 = 160 (amu)
Phần trăm khối lượng các nguyên tố trong CuSO4 là:
II. Hóa trị
1. Cách xác định hóa trị
Giải KHTN 7 trang 42
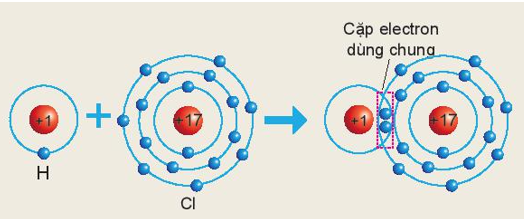
Câu hỏi trang 42 Khoa học tự nhiên 7: Sơ đồ sau mô tả sự hình thành liên kết cộng hóa trị trong phân tử HCl:
Xác định hóa trị của chlorine trong hợp chất trên.
Lời giải:
Trong chất cộng hóa trị, hóa trị của nguyên tố được xác định bằng số cặp electron dùng chung của nguyên tử nguyên tố đó với nguyên tử khác.
Theo sơ đồ mô tả sự hình thành liên kết cộng hóa trị trong phân tử HCl ta thấy:
Nguyên tử Cl có 1 cặp electron dùng chung với nguyên tử H ⇒ Trong hợp chất trên Cl có hóa trị I.
2. Quy tắc hóa trị
Hoạt động trang 42 Khoa học tự nhiên 7: Tìm hiểu về quy tắc hóa trị
Quan sát Bảng 7.1 và thực hiện các yêu cầu sau:
Bảng 7.1.
|
|
Hóa trị của lưu huỳnh/carbon |
Tích của chỉ số và hóa trị của lưu huỳnh/carbon |
Tích của chỉ số và hóa trị của hydrogen |
|
H2S |
II |
1.II |
2.I |
|
CH4 |
IV |
1.IV |
4.1 |
1. Xét phân tử H2S, hãy so sánh tích của chỉ số và hóa trị của nguyên tố lưu huỳnh với tích của chỉ số và hóa trị của nguyên tố hydrogen.
2. Đối với phân tử CH4, hãy so sánh tích của chỉ số và hóa trị của nguyên tố carbon với tích chỉ số và hóa trị của nguyên tố hydrogen.
Lời giải:
1. Xét phân tử H2S
Ta thấy: 1.II = 2.I
⇒ Tích của chỉ số và hóa trị của nguyên tố lưu huỳnh bằng tích của chỉ số và hóa trị của nguyên tố hydrogen.
2. Xét phân tử CH4.
Ta thấy: 1.IV = 4.I
⇒ Tích của chỉ số và hóa trị của nguyên tố carbon bằng tích của chỉ số và hóa trị của nguyên tố hydrogen.
Giải KHTN 7 trang 43
Câu hỏi 1 trang 43 Khoa học tự nhiên 7: Xác định hóa trị của lưu huỳnh trong hợp chất sulfur dioxide (một nguyên tử S liên kết với hai nguyên tử O).
Lời giải:
Oxygen được quy ước có hóa trị II.
Hợp chất sulfur dioxide (SO2), nguyên tử nguyên tố S liên kết được với hai nguyên tử O nên có hóa trị IV
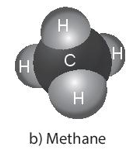
Câu hỏi 2 trang 43 Khoa học tự nhiên 7: Hãy xác định hóa trị của carbon trong hợp chất methane có trong Hình 5.3b.
Lời giải:
Quy ước nguyên tố H có hóa trị I.
Nguyên tử C liên kết được với 4 nguyên tử H nên nguyên tử C có hóa trị IV.
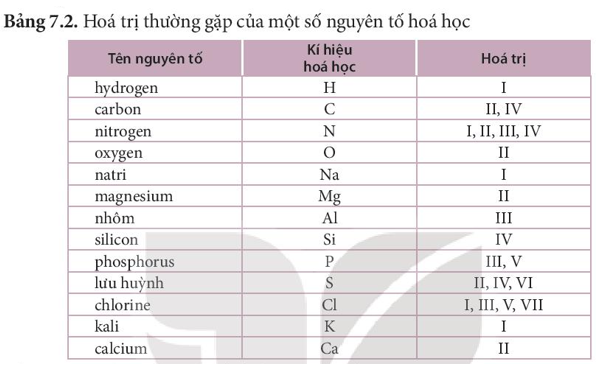
Câu hỏi 3 trang 43 Khoa học tự nhiên 7: Dựa vào quy tắc hóa trị và Bảng 7.2, cho biết công thức hóa học của potassium oxide là KO hay K2O.
Lời giải:
Theo bảng 7.2, nguyên tố K có hóa trị I, nguyên tố O có hóa trị II.
Giả sử, công thức hóa học của potassium oxide là KO.
Theo quy tắc hóa trị: 1.I ≠ 1.II
⇒ Giả sử sai.
⇒ Công thức hóa học của potassium oxide là K2O
Theo quy tắc hóa trị: 2.I = 1.II (thỏa mãn).
III. Lập công thức hóa học của hợp chất
2. Lập công thức hóa học của hợp chất theo phần trăm các nguyên tố
Giải KHTN 7 trang 44
Câu hỏi 1 trang 44 Khoa học tự nhiên 7: Khí carbon dioxide luôn có thành phần như sau: cứ 1 phần khối lượng carbon có tương ứng 2,667 phần khối lượng oxygen. Hãy lập công thức hóa học của khí carbon dioxide, biết khối lượng phân tử của nó là 44 amu.
Lời giải:
Đặt công thức của khí carbon dioxide là CxOy.
Khối lượng phân tử của khí carbon dioxide là: 12.x + 16.y = 44
Ta có:
Thay y = 2x vào phương trình khối lượng phân tử được:
12.x + 16.2x = 44 ⇒ x = 1, vậy y = 2.
Vậy công thức của khí carbon dioxide là CO2.
Câu hỏi 2 trang 44 Khoa học tự nhiên 7: Hãy lập công thức phân tử của khí hydrogen sulfide, biết lưu huỳnh trong hợp chất này có hóa trị II. Tính thành phần phần trăm về khối lượng của lưu huỳnh và của hydrogen trong hợp chất đó.
Lời giải:
Đặt công thức của khí hydrogen sulfide là
Theo quy tắc hóa trị: x.I = y.II
⇒
Lấy x = 2 và y = 1.
Vậy công thức của khí hydrogen sulfide là H2S.
⇒ Khối lượng phân tử của khí hydrogen sulfide là: 2.1 + 32 = 34 (amu).
Phần trăm về khối lượng của lưu huỳnh và của hydrogen trong H2S là:
Em có thể trang 44 Khoa học tự nhiên 7: Xác định được phần trăm khối lượng các nguyên tố hóa học có trong các chất dựa vào công thức phân tử trên nhãn mác sản phẩm như phân bón, thức ăn, đồ uống, …
Lời giải:
Bột thuốc muối chữa đau dạ dày có công thức hóa học là NaHCO3 (natri hydrocarbonat hay sodium hydrocarbonate).
Khối lượng phân tử NaHCO3 bằng 23.1 + 1.1 + 12 + 16.3 = 84 amu
Phần trăm khối lượng các nguyên tố hóa học trong NaHCO3 là:
%O = 100% – 27,38% – 1,19% – 14,29% = 57,14%
Bài giảng Khoa học tự nhiên lớp 7 Kết nối tri thức
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 7 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Bài 6: Giới thiệu về liên kết hóa học
Bài 8: Tốc độ chuyển động
Bài 9: Đo tốc độ
Bài 10: Đồ thị quãng đường – thời gian
Bài 11: Thảo luận về ảnh hưởng của tốc độ trong an toàn giao thông
Đăng bởi: THCS Bình Chánh
Chuyên mục: Khoa học tự nhiên 7 Kết nối tri thức
- Khoa học tự nhiên 7 Bài 1 Kết nối tri thức: Phương pháp và kĩ năng học tập môn khoa học tự nhiên | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 2 Kết nối tri thức: Nguyên tử | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 3 Kết nối tri thức: Nguyên tố hóa học | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 4 Kết nối tri thức: Sơ lược về bảng tuần hoàn các nguyên tố hóa học | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 5 Kết nối tri thức: Phân tử – Đơn chất – Hợp chất | Giải KHTN 7
- Khoa học tự nhiên 7 Bài 6 Kết nối tri thức: Giới thiệu về liên kết hóa học | Giải KHTN 7