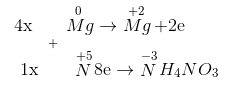Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Mời các em theo dõi nội dung bài học Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O do thầy cô trường THCS Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn.
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O được THCS Bình Chánh biên soạn hướng dẫn bạn đọc viết và cân bằng phương trình phản ứng oxi hóa khử Mg tác dụng HNO3 sản phẩm khử sinh ra là muối NH4NO3.
>> Mời các bạn tham khảo thêm một số nội dung liên quan:
Bạn đang xem: Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
- Mg + H2SO4 → MgSO4 + H2
- Mg + HNO3 → Mg(NO3)2 + NO2 + H2O
- Mg + HNO3 → Mg(NO3)2 + N2O + H2O
- Mg + HNO3 → Mg(NO3)2 + NO + H2O
- Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
- Mg + HNO3 → Mg(NO3)2 + N2 + H2O
- Mg + HNO3 → Mg(NO3)2 + NO + H2O
- MgO + HCl → MgCl2 + H2O
- Mg(OH)2 + HCl → MgCl2 + H2O
1. Phương trình phản ứng Mg + HNO3 ra NH4NO3
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
2. Cân bằng phản ứng Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Mg0 + HN+5O3 → Mg+2(NO3)2 + N-3H4NO3 + H2O
Tỉ lệ 2 muối nitrat của amoni và magiê là 1:4.
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
3. Điều kiện để phản ứng Mg tác dụng HNO3 loãng ra NH4NO3
Nhiệt độ thường
4. Bài tập vận dụng liên quan
Câu 1. Cho phương trình: Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Tổng hệ số cân bằng tối giản của phản ứng trên là
A. 23
B. 24
C. 18
D. 22
Xem đáp ánĐáp án D
Phương trình phản ứng hóa học
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
Tổng hệ số cân bằng tối giản của phản ứng trên là 22
Câu 2. Cho Mg tan hoàn toàn trong dung dịch HNO3 loãng không thấy có khí thoát ra . Trong phương trình phản ứng tổng hệ số của các chất (nguyên, tối giản) là bao nhiêu?
A. 20
B. 24
C. 25
D. 22
Xem đáp ánĐáp án D
Câu 3. Cho 4,8 gam Mg tác dụng với dung dịch HNO3 dư. Sau khi phản ứng xảy ra hoàn toàn thu được 1,792 lít NO (đktc) và dung dịch X. Khối lượng muối khan thu được khi cô cạn dung dịch X là
A. 13,92 gam
B. 15,60 gam
C. 16,80 gam
D. 31,20 gam
Xem đáp ánĐáp án D
Ta có:
nMg = 0,2 mol
nNO = 0,08 mol
Các quá trình trao đổi electron
Mg0 → Mg+2 + 2e
0,2 → 0,4
N+5 + 3e→ N+2
0,24 ← 0,08
Vậy còn 1 sản phẩm khử nữa là NH4NO3
N+5 + 8e → N-3
8x → x
Áp dụng bảo toàn electron ta có:
0,4 = 0,24 + 8x → a = 0,02 mol
=> mmuối = mNH4NO3 + mMg(NO3)2 = 31,2 gam
Câu 4. Hòa tan hỗn hợp gồm 2,7 gam Al và 13 gam Zn bằng 500 ml dung dịch HNO3 vừa đủ, thu được dung dịch X và không thấy khí thoát ra. Cô cạn dung dịch X thu a gam muối. Giá trị của a:
A. 66,1 gam
B. 68,2 gam
C. 43,4 gam
D. 33,1 gam
Xem đáp ánĐáp án A
nAl = 2,7/27 = 0,1 mol
nZn = 13/65 = 0,2 mol
Không thấy khí thoát ra => Sản phẩm khử là NH4NO3
⇒ nNH4NO3 = (0,1.3 + 0,2.2)/8 = 0,7/8 mol
Dung dịch muối X gồm: Al(NO3)3 (0,1 mol); Zn(NO3)2 (0,2 mol), NH4NO3 (0,7/8 mol)
m = mAl(NO3)3 + mZn(NO3)2 + mNH4NO3 = 0,1.213 + 0,2.189 + (0,7/8).80 = 66,1 gam
Câu 5. Cho các nhận xét dưới đây
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
(b) Đồng (Cu) không khử được muối sắt(III) (Fe3+).
(c) Ăn mòn kim loại là một quá trình hoá học trong đó kim loại bị ăn mòn bởi các axit trong môi trường không khí.
(d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Số nhận định đúng là
A. 2.
B. 3.
C. 4.
D. 1.
Xem đáp ánĐáp án A
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
( d ) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm .
Câu 6. Cho dãy các dung dịch: MgCl2 , AlCl3 , Na 2CO 3, NaHCO3, NH4Cl, BaCl2 . Số chất trong dãy tác dụng được với dung dịch NaOH là:
A. 3
B. 5
C. 2
D. 4
Xem đáp ánĐáp án D
Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch: sản phẩm có chất kết tủa hoặc chất bay hơi hoặc chất điện li yếu.
Giải chi tiết:
Có 4 dung dịch có phản ứng với NaOH:
MgCl2: MgCl2 + 2NaOH → Mg(OH)2 ↓ + 2NaCl
AlCl3: AlCl3 + 3NaOH → Αl(OH)3 ↓ + 3NaCl
Αl(OH)3 + NaOH → NaAlO2 + 2H2O
NaHCO3: NaHCO3 + NaOH → Na2CO3 + H2O
NH4Cl: NH4Cl + NaOH → NaCl + NH3 ↑ + H2O
Câu 7. Cho dãy các chất sau: Al, NaHCO3, (NH4)2CO3 , NH4Cl, Al2O3 , Zn, K2CO3 , K2SO4. Có bao nhiêu chất trong dãy vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch NaOH?
A. 2
B. 3
C. 4
D. 5
Xem đáp ánĐáp án D
Chất vừa tác dụng được với axit vừa tác dụng với bazơ gồm : các kim loại Al, Zn, Sn, Be, Pb,.. và các chất lưỡng tính và các muối có khả năng tạo kết tủa…
Chất lưỡng tính:
+ Là oxit và hidroxit của các kim loại Al, Zn, Sn, Pb; Cr(OH)3 và Cr2O3.
+ Là các ion âm còn chứa H có khả năng phân li ra ion H+ của các chất điện li trung bình và yếu ( HCO3–, HPO42-, HS–…)
( chú ý : HSO4– có tính axit do đây là chất điện li mạnh)
+ Là muối chứa các ion lưỡng tính; muối tạo bởi hai ion, một ion có tính axit và một ion có tính bazơ ( (NH4)2CO3…)
Vậy ta có 5 chất thỏa mãn là : Al, NaHCO3, (NH4)2CO3 , Al2O3, Zn.
………………………….
Trên đây THCS Bình Chánh.com vừa giới thiệu tới các bạn phương trình phản ứng Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O, mong rằng qua bài viết này các bạn có thể học tập tốt hơn môn Hóa học lớp 11.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, THCS Bình Chánh mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
Đăng bởi: THCS Bình Chánh
Chuyên mục: Học Tập