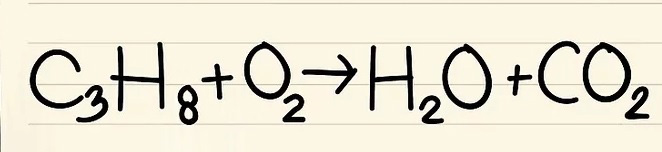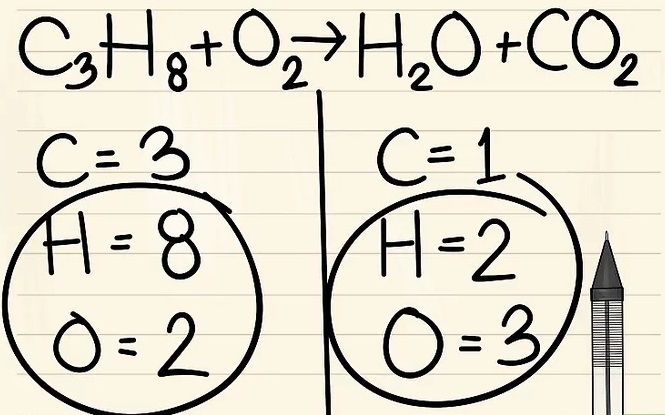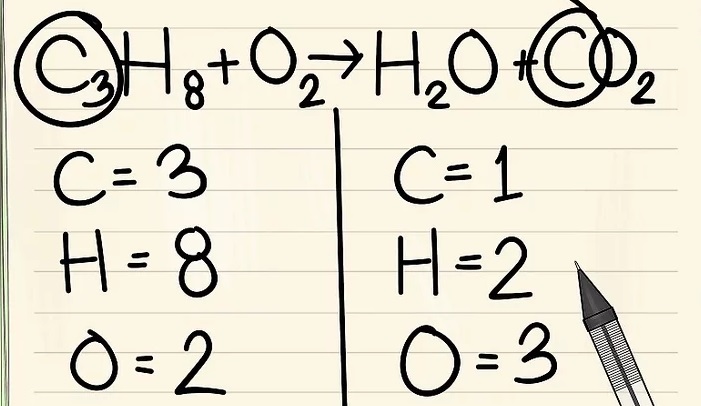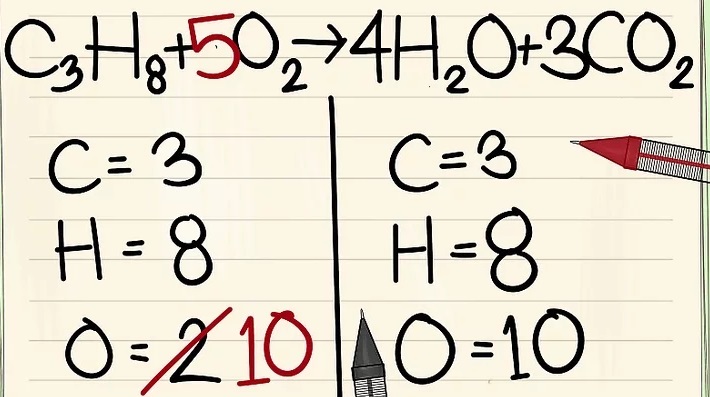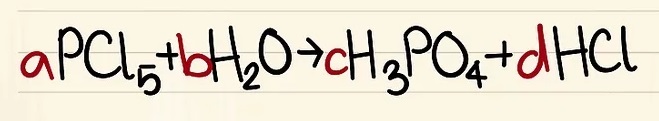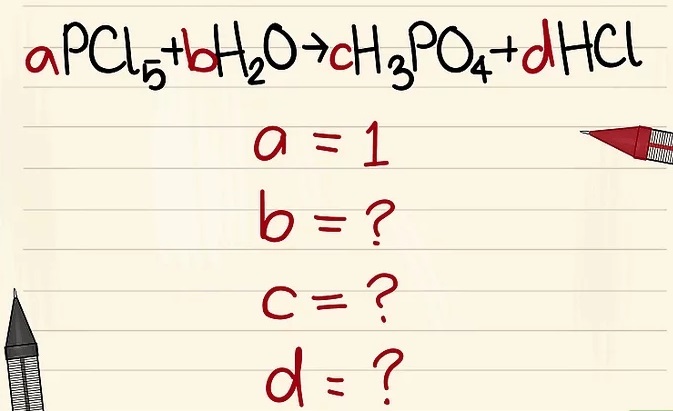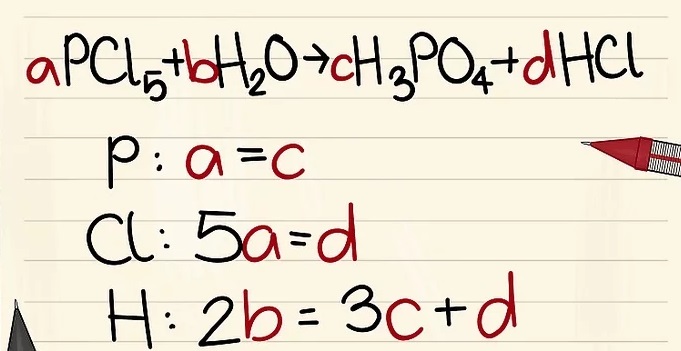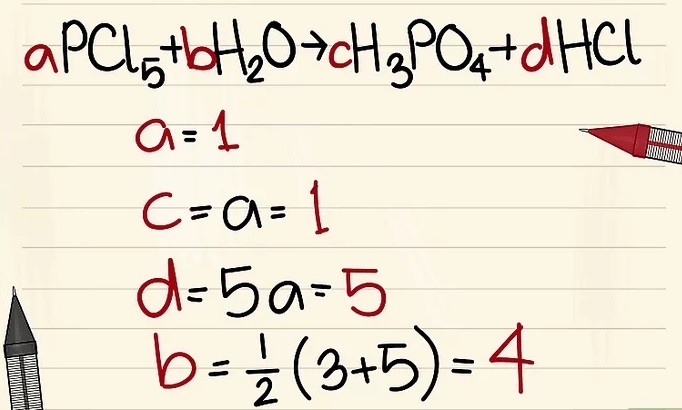Cách để Cân bằng Phương trình Hóa học
Mời các em theo dõi nội dung bài học Cách để Cân bằng Phương trình Hóa học do thầy cô trường THCS Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn.
Cách để Cân bằng Phương trình Hóa học
Cách để Cân bằng Phương trình Hóa học lớp 8
Cách để Cân bằng Phương trình Hóa học được THCS Bình Chánh sưu tầm và đăng tải. Hy vọng sẽ giúp ích cho các bạn học sinh củng cố kiến thức Hóa lớp 8. Mời các bạn cùng tham khảo
- Phản ứng hóa học của Kẽm (Zn) và Hợp chất của Kẽm – Cân bằng phương trình hóa học
- Phản ứng hóa học của Mangan (Mn) và Hợp chất của Mangan – Cân bằng phương trình hóa học
- Phản ứng hóa học của Vàng (Au) và Hợp chất của Vàng – Cân bằng phương trình hóa học
- Phản ứng hóa học của Crom (Cr) và Hợp chất của Crom – Cân bằng phương trình hóa học
I. Cân bằng theo phương pháp truyền thống
Bạn đang xem: Cách để Cân bằng Phương trình Hóa học
1. Viết phương trình đã cho. Ở ví dụ này, bạn sẽ có:
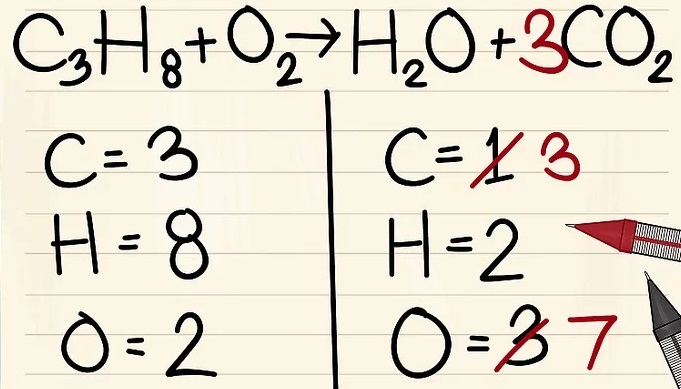
- C3H8 + O2 –> H2O + CO2
- Phản ứng này xảy ra khi prôban (C3H8) được đốt cháy trong ôxy để tạo thành nước và cacbon điôxít.
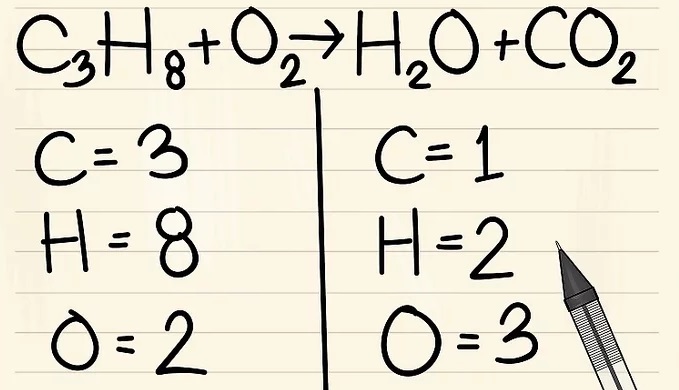
2. Viết số lượng nguyên tử của mỗi nguyên tố mà bạn có ở mỗi bên phương trình. Xem các chỉ số dưới bên cạnh mỗi nguyên tử để tìm ra số lượng nguyên tử trong phương trình.
- Bên trái: 3 cacbon, 8 hyđrô và 2 ôxy.
- Bên phải: 1 cacbon, 2 hyđrô và 3 ôxy.
3. Luôn để hyđrô và ôxy cuối cùng.
4. Nếu bạn còn lại nhiều hơn một nguyên tố để cân bằng: hãy chọn nguyên tố xuất hiện chỉ trong phân tử đơn của chất phản ứng và chỉ trong phân tử đơn của sản phẩm. Điều này có nghĩa rằng bạn sẽ cần phải cân bằng các nguyên tử cacbon trước.
5. Thêm hệ số cho đơn nguyên tử cacbon vào bên phải của phương trình để cân bằng nó với 3 nguyên tử cacbon ở bên trái của phương trình.
- C3H8 + O2 –> H2O + 3CO2
- Hệ số 3 đứng trước cacbon ở phía bên phải chỉ ra có 3 nguyên tử cacbon giống như chỉ số dưới 3 ở phía bên trái cho biết có 3 nguyên tử cacbon.
- Trong phương trình hóa học, bạn có thể thay đổi hệ số, nhưng không thể thay đổi chỉ số dưới.
6. Tiếp đến là cân bằng nguyên tử hyđrô. Bạn có 8 nguyên tử hyđrô ở bên trái. Do đó bạn sẽ cần có 8 ở bên phải.
- C3H8 + O2 –> 4H2O + 3CO2
- Ở bên phải giờ bạn thêm 4 làm hệ số vì chỉ số dưới cho biết bạn đã có 2 nguyên tử hyđrô.
- Khi bạn nhân hệ số 4 với chỉ số 2, bạn có 8.
- 6 nguyên tử Ôxy khác là từ 3CO2.(3×2=6 nguyên tử ôxy+ 4 nguyên tử ôxy khác=10)
7. Cân bằng các nguyên tử ôxy.
- Bởi vì bạn đã thêm hệ số vào các phân tử bên phải phương trình nên số nguyên tử ôxy đã thay đổi. Giờ bạn có 4 nguyên tử ôxy trong phân tử nước và 6 nguyên tử ôxy trong phân tử cacbon điôxít. Tổng cộng ta có 10 nguyên tử ôxy.
- Thêm hệ số 5 vào phân tử ôxy ở bên trái phương trình. Giờ bạn có 10 phân tử ôxy ở mỗi bên.
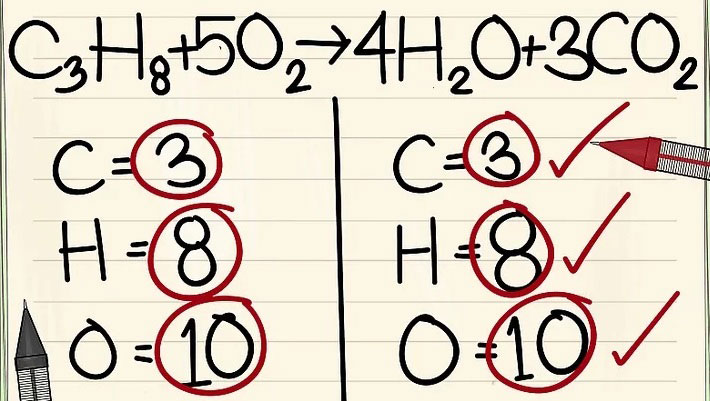
- C3H8 + 5O2 –> 4H2O + 3CO2
- Các nguyên tử cacbon, hyđrô, và ôxy được cân bằng. Phương trình của bạn đã hoàn tất.
II. Cân bằng theo phương pháp đại số
1. Viết phương trình theo ký hiệu và công thức. Ví dụ a=1 và viết phương trình dựa trên công thức đó.
2. Thay thế các chữ số bằng biến số của chúng.
3. Kiểm tra số lượng các nguyên tố có trong bên phản ứng cũng như bên sản phẩm.
- Ví dụ: aPCl5 + bH2O = cH3PO4 + dHCl để a=1 b= c= d= và tách các nguyên tố là P, Cl, H, O, vì vậy bạn được a=1 b=4 c=1 d=5.
Lời khuyên
Hãy nhớ giản lược phương trình.
Nếu bạn gặp khó khăn, bạn có thể gõ phương trình vào trong công cụ cân bằng trực tuyến để cân bằng nó. Hãy nhớ là khi đi thi bạn không được sử dụng công cụ cân bằng trực tuyến, do đó đừng lệ thuộc vào nó.
Cảnh báo
Đừng bao giờ sử dụng hệ số là phân số trong phương trình hóa học –bạn không thể chia đôi phân tử hoặc nguyên tử trong phản ứng hóa học.
Trong quá trình cân bằng, bạn có thể sử dụng phân số nhưng phương trình sẽ không được cân bằng nếu các hệ số vẫn là phân số.
Để loại bỏ phân số, nhân toàn bộ phương trình (cả bên trái và bên phải) với mẫu số của phân số.
……………………………………..
Ngoài Cách để Cân bằng Phương trình Hóa học. Mời các bạn học sinh còn có thể tham khảo các đề thi học kì 1 lớp 8, đề thi học kì 2 lớp 8 các môn Toán, Văn, Anh, Lý, Địa, Sinh mà chúng tôi đã sưu tầm và chọn lọc. Với tài liệu lớp 8 sẽ giúp các bạn ôn tập tốt hơn. Chúc các bạn học tập tốt
Đăng bởi: THCS Bình Chánh
Chuyên mục: Học Tập
- Cao Bá Quát là ai? Những chuyện ít người biết về Cao Bá Quát
- 1 đại đội có bao nhiêu người? Các đại đội của Quân đội Nhân dân Việt Nam
- 1 Lunatic 1 Ice Pick là gì? Video gây án khiến cả thế giới phải rúng động
- 100+ Ca dao tục ngữ về thầy cô hay và ý nghĩa
- 1001 Hình ảnh tình yêu hạnh phúc đẹp lãng mạn tặng lứa đôi
- 20 mẫu kết bài Chiếc thuyền ngoài xa hay nhất
- 63 trò chơi dân gian ngày Tết hay nhất dành cho Thiếu nhi
- 916 nghĩa là gì? Khi nào thì nên sử dụng con số 916?