Giải Hóa 10 Bài 4 trang 21, 22, 23, 24, 25 Cánh diều
Mời các em theo dõi nội dung bài học hôm nay Giải hóa 10 bài 4 trang 21, 22, 23, 24, 25 Cánh diều
Trong lịch sử các thuyết về mô hình nguyên tử, có mô hình hành tinh nguyên tử và mô hình hiện đại nguyên tử
Electron chuyển từ lớp gần hạt nhân ra lớp xa hạt nhân thì phải thu hay giải phóng năng lượng? Giải thích.
Dựa theo mô hình nguyên tử của Rutherford – Bohr, hãy vẽ mô hình nguyên tử các nguyên tố có Z từ 1 đến 11
Bạn đang xem: Giải Hóa 10 Bài 4 trang 21, 22, 23, 24, 25 Cánh diều
CH tr 21 MĐ
|
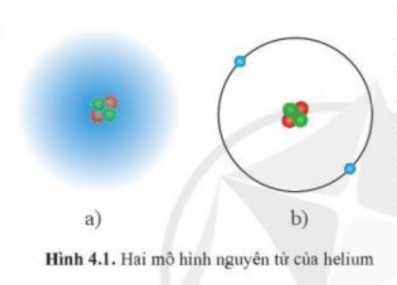
Trong lịch sử các thuyết về mô hình nguyên tử, có mô hình hành tinh nguyên tử và mô hình hiện đại nguyên tử. Theo em, trong hai hình bên, hình nào thể hiện mô hình hành tinh nguyên tử, hình nào thể hiện mô hình hiện đại của nguyên tử? |
Hướng dẫn giải:
– Hình a không mô tả sự chuyển động của electron
– Hình b mô tả sự chuyển động của electron
Lời giải:
– Mô hình hành tinh nguyên tử mô tả về sự chuyển động của electron.
– Hình a không mô tả sự chuyển động của electron
– Hình b mô tả sự chuyển động của electron
=> Hình b thể hiện mô hình hành tinh nguyên tử và Hình a thể hiện mô hình hiện đại của nguyên tử
CH tr 21 CH
|
Electron chuyển từ lớp gần hạt nhân ra lớp xa hạt nhân thì phải thu hay giải phóng năng lượng? Giải thích. |
Hướng dẫn giải:
Năng lượng của electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. Electron ở càng xa hạt nhân thì năng lượng càng cao.
Lời giải:
– Electron ở càng xa hạt nhân thì năng lượng càng cao
=> Electron ở gần hạt nhân có mức năng lượng thấp hơn electron ở xa hạt nhân
=> Electron cần phải thu năng lượng để có thể chuyển từ lớp gần ra lớp xa hạt nhân
CH tr 22 LT
|
1. Dựa theo mô hình nguyên tử của Rutherford – Bohr, hãy vẽ mô hình nguyên tử các nguyên tố có Z từ 1 đến 11. |
Hướng dẫn giải:
– Các electron được phân bố vào lớp gần hạt nhân trước.
– Số electron tối đa trong mỗi lớp là 2n2(n là số thứ tự lớp n $ \leqslant $ 4)
Lời giải:
CH tr 23 CH
|
2. Theo em, xác suất tìm thấy electron trong toàn phần không gian bên ngoài đám mây là khoảng bao nhiêu phần trăm. |
Hướng dẫn giải:
Xác suất tìm thấy electron trong đám mây là khoảng 90%, nghĩa là electron chuyển động khắp nơi trong không gian xung quanh hạt nhân nguyên tử, nhưng tập trung phần lớn ở khu vực này.
Lời giải:
Xác suất tìm thấy electron trong toàn phần không gian bên ngoài đám mây là khoảng 10%
CH tr 23 CH
|
Khái niệm AO xuất phát từ mô hình Rutherford – Bohr hay mô hình hiện đại về nguyên tử? |
Hướng dẫn giải:
– Orbital nguyên tử (AO) là khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%).
– Các electron chuyển động rất nhanh và sự chuyển động này tạo nên hình ảnh giống một đám mây electron.
Lời giải:
Khái niệm AO xuất phát từ mô hình hiện đại nguyên tử.
CH tr 23 CH
|
Chọn phát biểu đúng về electron s. A. Là electron chuyển động chủ yếu trong khu vực không gian hình cầu. B. Là electron chỉ chuyển động trên một mặt cầu. C. Là electron chỉ chuyển động trên một đường tròn. |
Hướng dẫn giải:
Electron s hay gọi là AO s là AO hình cầu.
Lời giải:
Đáp án đúng: A.
Bài tập 1
|
Bài 1: Những phát biểu nào sau đây là đúng khi nói về mô hình Rutherford – Bohr? A. Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời. B. Electron không chuyển động theo quỹ đạo cố định mà trong cả khu vực không gian xung quanh hạt nhân. C. Electron không bị hút vào hạt nhân do còn chịu tác dụng của lực quán tính li tâm. |
Hướng dẫn giải:
– Mô hình nguyên tử Rutherford – Bohr có nội dung:
+ Quỹ đạo quay của electron.
+ Lực quán tính li tâm.
Lời giải:
A. Đúng vì theo mô hình Rutherford – Bohr thì electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
B. Sai vì theo mô hình hiện đại thì electron chuyển động xung quanh hạt nhân không theo những quỹ đạo cố định.
C. Đúng vì theo mô hình Rutherford – Bohr, các electron mang điện tích âm nhưng không bị hút vào hạt nhân bởi lực hút này cân bằng với lực quán tính li tâm.
Bài tập 2
|
Bài 2: Nguyên tử Li (Z = 3) có 2 electron ở lớp K và 1 electron ở lớp L. So sánh năng lượng của electron giữa hai lớp theo mô hình Rutherford – Bohr. |
Hướng dẫn giải:
Theo mô hình Rutherford – Bohr electron ở càng xa hạt nhân thì có năng lượng càng cao.
Lời giải:
Năng lượng của electron của lớp K thấp hơn năng lượng của electron ở lớp L.
Bài tập 3
|
Bài 3: Sử dụng mô hình Rutherford – Bohr, hãy cho biết khi electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hay tiến gần vào hạt nhân hơn. Giải thích. |
Hướng dẫn giải:
Theo mô hình Rutherford – Bohr electron ở càng xa hạt nhân thì có năng lượng càng cao.
Lời giải:
Electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hạt nhân hơn do năng lượng càng cao thì electron ở càng xa hạt nhân.
Bài tập 4
|
Bài 4: Từ khái niệm: Orbital nguyên tử là khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%). Phát biểu sau đây có đúng không: Xác suất tìm thấy electron tại mỗi điểm trong không gian của AO là 90%. |
Hướng dẫn giải:
Khái niệm orbital nguyên tử (AO).
Lời giải:
Đúng vì xác suất tìm thấy electron trong khu vực không gian của AO là lớn nhất (khoảng 90%).
Bài tập 5
|
Bài 5: Trả lời những câu hỏi sau đây liên quan đến mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử. a) Vì sao còn gọi mô hình Rutherford – Bohr là mô hình hành tinh nguyên tử? b) Theo mô hình hiện đại, orbital p có hình số tám nổi với hai phần (còn gọi là hai thùy) giống hệt nhau. Xác suất tìm thấy electron ở mỗi thùy là khoảng bao nhiêu phần trăm? c) So sánh sự giống và khác nhau giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử. |
Hướng dẫn giải:
– Mô hình Rutherford – Bohr.
– Mô hình hiện đại về nguyên tử.
Lời giải:
a) Vì mô hình biểu diễn electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời nên được gọi là mô hình hành tinh nguyên tử.
b) Xác suất tìm thấy electron ở mỗi thùy của orbital p là khoảng 90%.
c)
Lý thuyết
>> Xem chi tiết: Lý thuyết bài 4: Mô hình nguyên tử và orbital nguyên tử
Hy vọng với nội dung trong bài Giải hóa 10 bài 4 trang 21, 22, 23, 24, 25 Cánh diều
do thầy cô trường Trung học Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn để từ đó hoàn thành tất cả các bài tập trong SGK.
Đăng bởi: THCS Bình Chánh
Chuyên mục: Hóa học 10 Cánh Diều
- Giải Hóa 10 Bài 1 trang 6, 7, 8, 9, 10 Cánh diều
- Giải Hóa 10 Bài 2 trang 11, 12, 13, 14, 15 Cánh diều
- Giải Hóa 10 Bài 3 trang 16, 17, 18, 19, 20 Cánh diều
- Giải Hóa 10 Bài 5 trang 26, 27, 28, 29, 30 Cánh diều
- Giải Hóa 10 Bài 6 trang 31, 32, 33, 34, 35, 36, 37 Cánh diều
- Giải Hóa 10 Bài 7 trang 38, 39, 40, 41, 42, 43, 44, 45 Cánh diều