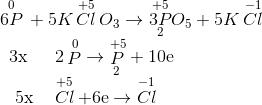P + KClO3 → KCl + P2O5
Mời các em theo dõi nội dung bài học P + KClO3 → KCl + P2O5 do thầy cô trường THCS Bình Chánh biên soạn sẽ giúp các em nắm chắc kiến thức nội dung bài học tốt hơn.
Mục lục
P + KClO3 → KCl + P2O5
P + KClO3 → KCl + P2O5 được THCS Bình Chánh biên soạn hướng dẫn bạn đọc viết và cân bằng phương trình phản ứng, cũng như chỉ ra P có tính khử hay tính oxi hóa. Từ đó bạn đọc nắm được nội dung, vận dụng giải các dạng câu hỏi bài tập liên quan.
>> Mời các bạn tham khảo một số phương trình liên quan
Bạn đang xem: P + KClO3 → KCl + P2O5
- P2O5 + H2O → H3PO4
- P2O5 + KOH → K3PO4 + H2O
- P + Cl2 → PCl3
- P + H2SO4 → H3PO4 + SO2 + H2O
- P + HNO3 → H3PO4 + NO2 + H2O
1. Phương trình phản ứng P ra P2O5
6P + 5KClO3 → 5KCl + 3P2O5
2. Cân bằng phản ứng P + KClO3 → KCl + P2O5
Xác định số oxi hóa thay đổi
Phương trình phản ứng hóa học
6P + 5KClO3 → 5KCl + 3P2O5
P đóng vai trò là chất khử
2. Điều kiện phản ứng P tác dụng với KClO3
Nhiệt độ cao
3. Câu hỏi vận dụng liên quan
Câu 1. Cho phản ứng: P + KClO3 → P2O5 + KCl. Hệ số cân bằng của phương trình phản ứng này từ trái qua phải lần lượt là:
A. 2, 1, 1, 1
B. 4, 3, 2, 3
C. 8, 1, 4, 1
D. 6, 5, 3, 5
Xem đáp ánĐáp án D
Câu 2. Photpho thể hiện tính oxi hóa ở phản ứng nào sau đây?
A. 2P + 5Cl2 2PCl5
B. 2P + 5O22P2O5
C. P + 5HNO3⟶ H3PO4 + 5NO2+ H2O
D. 3Ca + 2P Ca3P2
Xem đáp ánĐáp án D
Câu 3. Trong phản ứng của photpho với (1) Ca, (2) O2, (3) Cl2, (4) KClO3. Những phản ứng trong đó photpho thể hiện tính khử là
A. (1), (2), (4).
B. (1), (3).
C. (2), (3), (4).
D. (1), (2), (3).
Xem đáp ánĐáp án C
Câu 4. Đốt cháy photpho trong khí clo dư, phản ứng xảy ra hoàn toàn, sau phản ứng ta thu được hợp chất nào?
A. PCl3
B. PCl5
C. PCl2
D. PCl6
Xem đáp ánĐáp án B
Câu 5. Phát biểu nào sau đây là sai?
A. cấu hình electron nguyên tử của photpho là 1s22s22p63s23p6.
B. Photpho chỉ tồn tại ở 2 dạng thù hình photpho đỏ và photpho trắng.
C. Photpho trắng hoạt động mạnh hơn photpho đỏ
D. Ở nhiệt độ thường photpho hoạt động mạnh hơn nitơ.
Xem đáp ánĐáp án B
B sai vì photpho có thể tồn tại ở nhiều dạng thù hình khác nhau nhưng quan trọng nhất là photpho trắng và photpho đỏ.
Câu 6. Hai khoáng vật chính của photpho là:
A. Apatit và hematit
B. Pirit và photphorit
C. Apatit và photphorit
D. Manhetit và apatit
Xem đáp ánĐáp án C
Câu 7. Cho sơ đò chuyển hóa: P2O5 → X → Y → Z. Các chất X, Y, Z lần lượt là
A. KH2PO4, K2HPO4, K3PO4
B. KH2PO4, K3PO4, K2HPO4
C. K3PO4, KH2PO4, K2HPO4,
D. K3PO4, K2HPO4, KH2PO4
Xem đáp ánĐáp án C
Câu 8. Thủy phân hoàn toàn 5,42 gam PX3 trong nước thu được dung dịch A. Trung hòa dung dịch A cần dùng 100 ml dung dịch NaOH 1M. Biết rằng H3PO3 là một axit 2 nấc. Công thức của PX3 là
A. PBr3.
B. PI3.
C. PF3.
D. PCl3.
Xem đáp ánĐáp án A
PX3 (x) + 3H2O → H3PO3 (x) + 3HX (3x mol)
2NaOH + H3PO3 → Na2HPO3 + 2H2O
NaOH + HX → NaX + H2O
nNaOH = 2nH3PO3 + nHX = 5x = 0,1 ⇒ x = 0,02 mol
PX3 = 5,42 : 0,02 = 271 ⇒ X = 80 ⇒ Br ⇒ PBr3
Câu 9. Photpho hoạt động hoá học mạnh hơn nitơ trong điều kiện thường là do
A. độ âm điện của photpho (2,2) nhỏ hơn của nitơ (3,0).
B. trong điều kiện thường photpho ở trạng thái rắn, còn nitơ ở trạng thái khí.
C. liên kết trong phân tử photpho kém bền hơn trong phân tử nitơ.
D. photpho có nhiều dạng thù hình, còn nitơ chỉ có một dạng thù hình.
Xem đáp ánĐáp án C
Trong điều kiện thường, photpho hoạt động hoá học mạnh hơn nitơ là do liên kết trong phân tử photpho kém bền hơn trong phân tử nitơ.
Câu 10. Khi đun nóng trong điều kiện không có không khí, photpho đỏ chuyển thành hơi, sau đó làm lạnh phần hơi thì thu được photpho
A. đỏ.
B. vàng.
C. trắng.
D. nâu.
Xem đáp ánĐáp án C
Khi đun nóng trong điều kiện không có không khí, photpho đỏ chuyển thành hơi, sau đó làm lạnh phần hơi thì thu được photpho trắng.
———————————–
Trên đây THCS Bình Chánh đã giới thiệu tới các bạn phương trình phản ứng: P + KClO3 → KCl + P2O5. Để có thể nâng cao kết quả trong học tập, THCS Bình Chánh xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 11, Chuyên đề Hóa học 11, Giải bài tập Hoá học 11. Tài liệu học tập lớp 11 mà THCS Bình Chánh tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, THCS Bình Chánh mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
Đăng bởi: THCS Bình Chánh
Chuyên mục: Học Tập